Número: 12.12 - 7 Artigo(s)
- Imprimir
- Indicar
- Estatísticas
- (0) Comentários
- Como Citar
- Download Citação
- Artigos Relacionados
- Outros dos Autores
Artigos Originais http://www.dx.doi.org/10.5935/2674-7960.v12-0001
Resistência aos antimicrobianos e seu impacto na saúde pública: uma revisão sistemática
Resistance to antimicrobials and their impact on public health: a systematic review
Adélia Ferreira de Souza1; Ana Paula Ferreira2; Thauana Sampaio Coelho Souza3; Viviane Pagliarini de Almeida4
1. Graduação em Farmácia. Faculdade Dinâmica do Vale do Piranga, (FADIP), Brasil
2. Graduou-se em Fisioterapia pela Faculdade de Ciências Médicas e da Saúde de Juiz de Fora (FCMS/JF), possui Doutorado em Ciências da Reabilitação pela Universidade Federal de Minas Gerais (UFMG). E-mail: paulaffisio@gmail.com . Brasil
3. Pós-Graduação - Farmacêutica Bioquímica do Exército Brasileiro (EB) - Brasil
4. Pós-graduação - Farmacêutica Bioquímica do Exército Brasileiro (EB) - Brasil
Recebido em 02/06/2023
Aceito em 17/08/2023
Resumo
INTRODUÇÃO: Antimicrobianos são fármacos de origem natural ou sintética, podem ser classificados como bactericida, quando causam a morte da bactéria, ou bacteriostático, quando promovem a inibição do crescimento microbiano. A resistência aos antibióticos se refere àqueles microrganismos cujo crescimento e multiplicação não se inibem pelas concentrações habitualmente alcançadas no sangue ou tecidos.
OBJETIVO: Analisar a resistência bacteriana causada pelo uso indiscriminado dos antimicrobianos.
MÉTODOS: Foram analisados os mais relevantes estudos, tendo como referência a base de dados MedLine (National Library of Medicine) e SciELO. Objetivando selecionar os estudos de maior evidência científica, foram selecionados apenas os ensaios clínicos e estudos observacionais.
RESULTADOS: Inicialmente foram identificados 121 estudos que investigaram a associação da resistência bacteriana devido ao uso indiscriminado de antimicrobianos. Contudo, após aplicação dos critérios de inclusão e exclusão, apenas cinco fizeram parte do escopo desta revisão.
CONCLUSÃO: A resistência bacteriana aos antimicrobianos representa uma ameaça grave à saúde pública global, devido ao seu uso abusivo e muitas das vezes desnecessário. Para que ocorra a mudança desses hábitos é importante promover uma educação sanitária para profissionais da saúde e para a população, assim evitando a automedicação e promovendo o uso correto dos mesmos.
Palavras-chave: Resistência a Medicamentos; Resistência a Medicamentos Antineoplásicos; Resistência a Antineoplásicos; Resistência Microbiana a Medicamentos; Interações Microbianas.
INTRODUÇÃO
Antibióticos são fármacos de origem natural ou sintética e podem ser classificados como bactericida, quando causam a morte da bactéria, ou bacteriostático, quando promovem a inibição do crescimento microbiano.(1) A sua utilização na prática clínica modificou o curso natural das doenças infecciosas, melhorando, assim, seu prognóstico.(2)
Desde a introdução do mais antigo antimicrobiano até o mais recente, nota-se que o equilíbrio existente entre o homem e as bactérias tem sido alterado pelo uso irracional e indiscriminado dessas drogas tanto nos cuidados com a saúde humana quanto com a saúde animal, podendo os microrganismos apresentar mecanismos de resistência intrínsecos e extrínsecos.(2,10)
A resistência pode ser considerada um fenômeno ecológico que ocorre como resposta da bactéria frente ao amplo uso de antibióticos e sua presença no meio ambiente.(3) O termo resistente se refere àqueles microrganismos cujo crescimento e multiplicação não se inibem pelas concentrações habitualmente alcançadas no sangue ou tecidos do correspondente antimicrobiano(2,11).
As principais consequências da resistência bacteriana são o aumento do tempo de hospitalização; aumento da frequência e da gravidade das infecções relacionadas à assistência à saúde; aumento da taxa de mortalidade associada a este tipo de infecção (3,12). De acordo com Gurgel et al. (2007)(3,12) as doenças infecciosas sempre foram um problema de saúde pública mundial, e o advento da terapia com antimicrobianos trouxe notável progresso ao tratamento das mesmas. Ainda segundo Gurgel et al. (2007)(3,14) bactérias importantes como Streptococcus pneumoniae, Haemophylus influenzae, Campylobacter jejuni, Staphylococcus aureus, Mycobacterium tuberculosis, Escherichia coli, Enterococcus sp., Shigella sp., Salmonella sp. e Vibrio cholerae apresentam cepas resistentes aos mais modernos antimicrobianos. Os antibióticos também são amplamente utilizados na produção animal como medida terapêutica no tratamento de infecções, como medida subterapêutica na prevenção de doenças e como promotores do crescimento(3).
Entretanto, por meio de estudos, dentre eles o dos autores Korb et al. (2011)(4) o emprego de antibióticos na pecuária, como forma de promotores de crescimento, tem a finalidade de proporcionar um melhor desenvolvimento do animal, porém, o antibiótico apresenta-se em baixas dosagens, numa concentração insuficiente para eliminar todas as bactérias patogênicas do organismo, e, com isso, esses microrganismos podem se adaptar levando ao aparecimento de linhagens bacterianas resistentes. Por meio do consumo de produtos de origem animal, como o leite, ou por meio das eliminações vesicais e intestinais, partes das bactérias acabam disseminando e ocasionando a resistência bacteriana nos seres humanos.
De acordo com Korb et al. (2011)(4) os dados que relacionam a problemática da resistência na pecuária com a saúde humana, e que destacam o fenômeno da resistência cruzada decorrente da semelhança entre antibióticos utilizados em seres humanos com os utilizados em animais, são escassos.
Guimarães et al. (2011)(1) evidenciaram que muitos protótipos não são adequados ao futuro desenvolvimento de fármacos devido a problemas relacionados à farmacocinética. Com estas características, ensaios baseados em modelos de infecção in vivo podem levar à identificação de novas substâncias ativas com maior quantidade de informações agregadas, o que pode agilizar o processo de desenvolvimento de eventuais antibióticos a partir de protótipos descobertos. Há uma consciência mundial do problema tornando este estudo importante e oportuno. Portanto, mediante o exposto, os objetivos do presente estudo foram analisar, por meio de revisão sistemática, a resistência bacteriana causada pelo uso indiscriminado dos antimicrobianos, discutir sobre os impactos sociais e econômicos causados pela resistência e reunir informações para conscientizar os profissionais de saúde e a população sobre o uso indiscriminado de antibióticos.
MÉTODOS
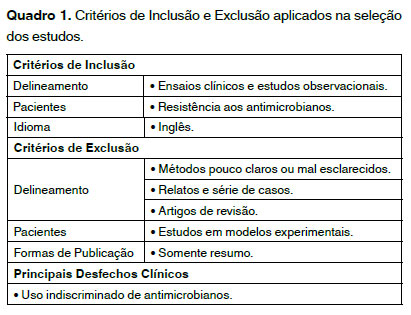
Foram analisados os mais relevantes estudos publicados originalmente na Língua Inglesa nos últimos 5 anos, tendo como referência a base de dados PubMed e SciELO. Objetivando pesquisar os estudos de maior evidência científica, foram selecionados apenas os ensaios clínicos e estudos observacionais Tabela 1.
A estratégia de busca utilizou as seguintes combinações de palavras-chave: (“Drug Resistance, Microbial”[Mesh]) AND “Microbial Resistance”. Para identificar os delineamentos dos estudos, foram empregados os seguintes termos: Observacional Study, Randomized Controlled Trial, Clinical Trial e Humans. Para a seleção dos estudos, foram aplicados os critérios de inclusão e exclusão apresentados no Quadro 1.
RESULTADOS
Inicialmente foram identificados 121 estudos que investigaram a associação da resistência bacteriana devido ao uso indiscriminado de antimicrobianos. Contudo, após aplicação dos critérios de inclusão e exclusão, apenas 5 fizeram parte do escopo desta Revisão. O fluxograma da seleção dos artigos que compõem a presente revisão, se encontra na Figura 1.
DISCUSSÃO
De acordo com os achados da presente revisão, foi observado que, nas últimas décadas, houve um aditamento na resistência bacteriana aos antibióticos, hoje considerada um problema de saúde pública mundial, devido ao uso indiscriminado e incorreto de antibióticos em nível hospitalar e comunitário, sem pormenorizar. Dados da Organização Mundial da Saúde (OMS), em 2001, já apontavam que mais de 50% das prescrições de antimicrobianos são inapropriadas e dois terços dos mesmos são usados sem prescrição médica em muitos países. Por conseguinte, atenuou-se, de forma proeminente, o número de drogas antibacterianas, hodiernamente elaboradas por indústrias farmacêuticas, que estão diligenciando para lograr novos agentes antimicrobianos, pois, o advento de bactérias panresistentes, que atingiu um nível alarmante, se fez, impreterível, a necessidade de elaborar novas classes de antimicrobianos compostos para abalizar os impasses no tocante à resistência microbiana.
Estudos que norteiam a prescrição e a utilização racional de antimicrobianos e que visam minimizar a resistência bacteriana têm sido objeto de muitas publicações segundo Mitre et al. (2018)(5,15) e Almaaytah et al. (2017)(6). De acordo com Costa et al. (2019)(7,16) a utilização de medicamentos pela população é um tema que faz parte das prioridades da OMS, e a RDC nº 20/2011 é uma medida de vigilância sanitária fundamental para a melhoria da qualidade de assistência à população. Contudo, a formalização da política em uma regulamentação, não garante o seu efetivo cumprimento. O controle da utilização adequada de medicamentos é uma questão antiga e de difícil operacionalização no Brasil, em razão de fatores de ordem econômica, cultural, de informação, educação e fiscalização.
De acordo com Sampaio et al. (2018)(8,16), a existência da RDC nº 20/2011 possibilita a diminuição do uso indiscriminado dos antimicrobianos e a minoração do uso inadequado desses medicamentos. Ribeiro et al. (2019)(7,17) confirmam que a incidência de infecção hospitalar por microrganismo é significantemente maior no período anterior à medida restritiva para comercialização de ATM (Antimicrobianos) em comparação ao período posterior. Poucos estudos têm sido realizados com o intuito de identificar as contribuições da medida restritiva no controle das infecções, sendo a maioria deles direcionada para a análise das vendas de ATM em drogarias e diminuição da resistência no ambiente comunitário. Para Ribeiro et al. (2019)(7,18), a restrição ao uso comunitário de ATM pode reduzir infecções hospitalares por microrganismos resistentes.
De acordo com Silva et al. (2020)9 , o uso de antimicrobianos em humanos ou animais, independente da quantidade ou finalidade promove pressão seletiva nas bactérias, tornando-as resistentes a tais medicamentos, o que favorece a disseminação da resistência antimicrobiana.
A OMS reconheceu a existência da relação entre o uso de antibióticos em animais e a resistência antimicrobiana em humanos com base em evidências que relataram o aparecimento de cepas bacterianas resistentes a antibióticos em humanos após a introdução desse medicamento na produção de alimentos de origem animal, pois houve um aumento na população mundial gerando um crescimento da demanda por esses alimentos(9).
Segundo Silva et al. (2020)(9,19) foi proposta a adoção de legislações para controlar o consumo de antibióticos na produção animal, tais como a obrigatoriedade da prescrição veterinária; reconhecendo que a resistência antimicrobiana é um problema complexo e multifatorial e requer a colaboração de diversos setores da sociedade, como médicos; médicos veterinários; farmacêuticos e outros profissionais da saúde; produtores agropecuários; indústria farmacêutica; sociedade civil; governos e outros atores interessados.
Proferindo inovações e consoante com Almaaytah et al. (2017)(6,20), os peptídeos antimicrobianos (AMP’s) ganharam grande interesse recentemente para servir como alternativas potenciais aos antibióticos convencionais, em virtude de suas propriedades únicas, como estruturas únicas, modos de ação e baixa probabilidade de induzir resistência microbiana. Os AMP’s são considerados excelentes alternativas aos antibióticos convencionais. A hipótese é que quando os AMP’s entram em contato com as membranas celulares, eles adotam estruturas anfifílicas que lhes permitem induzir a formação de poros nas membranas alvo e, consequentemente, causar a morte celular. Os AMP’s exibem uma baixa tendência de induzir resistência bacteriana, com atividades antimicrobianas de amplo espectro rápidas e potentes contra uma ampla gama de organismos envolvendo bactérias Gram-negativas e Gram-positivas multirresistentes, parasitas, fungos e vírus, testificando a estes AMP’s, propriedades atraentes com maior seletividade e atividade para patógenos. Lastimavelmente, muitos obstáculos deslindaram seu desenvolvimento e uso clínico. Esses senões são atribuídos à baixa estabilidade em fluidos biológicos, devido à inativação por lipoproteínas e albuminas aniônicas. Ademais, os AMP’s têm seletividade de alvo antimicrobiano restrita, o que leva a interações indesejáveis com macromoléculas do hospedeiro e alta toxicidade sistêmica, convergindo a maioria dos esforços de pesquisa em melhorar a estabilidade do AMP e reduzir a toxicidade sistêmica.
Nessa perspectiva, o encapsulamento de AMP’s por nanoestruturas pode representar uma abordagem inovadora para superar alguns problemas relacionados ao uso cerceado desses peptídeos, clinicamente. Destarte, os AMP’s catiônicos ultracurtos (USAMP’s) que consistem em menos de oito resíduos são um grupo promissor de AMP’s que atendem aos critérios necessários para o desenvolvimento de novos medicamentos antimicrobianos devido ao seu modo de ação incomparável, que é resultado de sua alta diversidade em relação ao comprimento do peptídeo, sequência de aminoácidos e estrutura. Outrossim, os USAMP’s exibem alta atividade antimicrobiana, com toxicidade insignificante ou muito baixa contra células hospedeiras de mamíferos. O desenvolvimento de USAMP’s também é atraente devido aos baixos custos de produção, menor probabilidade de desenvolver resistência e toxicidade hemolítica irrisória quando comparado com os AMP’s convencionais relatados na literatura. O custo de produção também é uma prerrogativa dessas moléculas, devido à sequência curta dos peptídeos, como versa o autor Almaaytah et al. (2017)(6,20).
CONCLUSÃO
A resistência bacteriana aos antimicrobianos representa uma ameaça grave à saúde pública global. Apesar de sua gênese multifatorial, um dos principais fatores que a desencadeia é o uso desnecessário e abusivo de antimicrobianos, fato extensivamente descrito na literatura internacional e nacional. Para que ocorram mudanças nos hábitos da população, a existência de legislações e regulamentações sobre o uso e prescrição de antimicrobianos é muito importante para evitar a automedicação e promover o uso correto dos mesmos. A educação sanitária para profissionais de saúde e para a população, bem como a fiscalização sanitária, devem ser efetivamente implementados, não apenas para alcançar o uso racional, mas também para diminuir a resistência aos antimicrobianos e consequentemente a redução da incidência de infecção hospitalar por microrganismos resistentes.
Há esperança de uma terapêutica revolucionária, por meio da qual os resultados demonstrem que o uso da nanotecnologia pode coibir o aumento e a propagação bacteriana, apresentando potentes atividades seletivas e de longa ação contra um extenso número de bactérias incluindo cepas resistentes. Por fim, essa nanotecnologia exerce mínima toxicidade, garantindo uma seletividade significativa contra células microbianas, quando comparada aos antibióticos convencionais.
Tendo em vista a complexidade da resistência, é necessário o uso racional de antibióticos tanto na saúde humana quanto na saúde animal. Pelo fato de a resistência bacteriana ser um problema de saúde pública, é possível concluir que a utilização correta dos antimicrobianos, indicados para uma condição clínica bem estabelecida, pode retardar o desenvolvimento da resistência bacteriana.
REFERÊNCIAS
1. Guimarães DO, Momesso LS, Pupo MT. Antibióticos: importância terapêutica e perspectivas para a descoberta e desenvolvimento de novos agentes. Quim Nova. 2012;33(3):667-79. doi: 10.1590/S0100-40422010000300035
2. Vieira PN, Vieira SLV. Uso irracional e resistência a antimicrobianos em hospitais. Arq Cienc Saúde Unipar. 2017;21(3):209-212. doi: 10.25110/arqsaude.v21i3.2017.6130
3. Gurgel TC, Carvalho WS. A Assistência Farmacêutica e o Aumento da Resistência Bacteriana aos Antimicrobianos. Lat Am J Pharm. 2008; 27(1):118-23.
4. Korb Arnildo, Brambilla DK, Teixeira DC, Rodrigues RM. Riscos para a saúde humana no uso de antibióticos na cadeia produtiva leiteira. Rev Saúde Públ Santa Cat. 2011;4(1).
5. Mitre GS, Silva AB, Silva GAB, Rezende MMPR, Junior JRS. Perfil de prescrição de antimicrobianos nas unidades básicas de saúde conveniadas com a universidade de Itaúna/MG. RMMG. 2018;27(1-6).
6. Almaaytah A, Mohammed GK, Abualhaijaa A, Al-Balas Q. Development of novel ultrashort antimicrobial peptide nanoparticles with potent antimicrobial and antibiofilm activities against multidrug-resistant bacteria. Drug Des Devel Ther. 2017 Nov 3;11:3159-3170. doi: 10.2147/DDDT.S147450
7. Costa JM, Moura CS, Pádua CAM, Vegi ASF, Magalhães SMS, Rodrigues MB, et al. Medida restritiva para comercialização de antimicrobianos no Brasil: resultados alcançados. Rev Saúde Pública. 2019;53:68. doi: 10.11606/s1518-8787.2019053000879
8. Sampaio PS, Sancho LG, Lago RF. Implementação da nova regulamentação para prescrição e dispensação de antimicrobianos: possibilidades e desafios. Cad Saúde Colet. 2018;26(1):15-22 doi: 10.1590/1414-462X201800010185
9. Silva RA, Oliveira BNL, Silva LPA, Oliveira MA, Chaves GC. Resistência a antimicrobianos: a formulação da resposta no âmbito da saúde global. Saúde Debate. 2020;44(126):607-23. doi: 10.1590/0103-1104202012602
10. Loureiro RJ, Roque F, Rodrigues AT, Herdeiro MT, Ramalheira E. O uso de antibióticos e as resistências bacterianas: breves notas sobre a sua evolução. Rev Port Saúde Pública. 2016; 34(1):77-84. doi: 10.1016/j.rpsp.2015.11.003
11. Aquino DS. Por que o uso racional de medicamentos deve ser uma prioridade? Ciên Saúde Coletiva. 2008;13(suppl):733-35. doi: 10.1590/S1413-81232008000700023
12. Silva CDR, Silva Júnior M. Estratégias para uso adequado de antibioticoterapia em unidade de terapia intensiva. Einstein (Sao Paulo). 2015;13(3):448-53. doi: 10.1590/S1679-45082015RW3145
13. Costa ALP, Silva Junior ACS. Resistência bacteriana aos antibióticos e saúde pública:uma breve revisão de literatura. Estação Científica. 2017;7(2): 45-57. doi: 10.18468/estcien.2017v7n2.p45-57
14. Mota RA, Silva KPC, Freitas MFL, Porto WJN, Silva LBG. Utilização indiscriminada de antimicrobianos e sua contribuição a multirresistência bacteriana. Braz J Vet Resanim Sci. 2005; 42(6):465-70. doi: 10.11606/issn.1678-4456.bjvras.2005.26406
15. Mota LM, Vilar FC, Dias LBA, Nunes TF, Moriguti JC. Uso racional de antimicrobianos. Rev Medicina (Ribeirão Preto). 2010;43(2):164-72. doi: 10.11606/issn.2176-7262.v43i2p164-172
16. Ministério da Saúde (BR). Agência Nacional de Vigilância Sanitária. Resolução da Diretoria Colegiada-RDC nº 44, de 26 de outubro de 2010. Dispõe sobre o controle de medicamentos à base de substâncias classificadas como antimicrobianos, de uso sob prescrição médica, isoladas ou em associação e dá outras providências. Available from:URL:https://bvsms.saude.gov.br/bvs/saudelegis/anvisa/2010/res0044_26_10_2010.html. Accessed May 15, 2021.
17. Ministério da Saúde (BR). Portaria Nº 2.616 de 12 de maio de 1998. Dispõe sobre o controle de infecções hospitalares. Available from: URL:http://bvsms.saude.gov.br/bvs/saudelegis/gm/1998/prt2616_12_05_1998.html. Accessed May 15, 2021.
18. Ministério da Saúde (BR). Agência Nacional de Vigilância Sanitária. Projeto de implantação da rede nacional de monitoramento da resistência microbiana em serviços de saúde. Available from: URL: http://www.anvisa.gov.br/servicosaude/hsentinela/projeto_rede_microbiana.pdf. Accessed May 15, 2021.
19. Dellit TH, Owens RC, McGowan JE Jr, Gerding DN, Weinstein RA, Burke JP, Huskins WC, Paterson DL, Fishman NO, Carpenter CF, Brennan PJ, Billeter M, Hooton TM; Infectious Diseases Society of America; Society for Healthcare Epidemiology of America. Infectious Diseases Society of America and the Society for Healthcare Epidemiology of America guidelines for developing an institutional program to enhance antimicrobial stewardship. Clin Infect Dis. 2007 Jan 15;44(2):159-77. doi: 10.1086/510393
20. Roscia G, Falciani C, Bracci L, Pini A. The development of antimicrobial peptides as new antibacterial drugs. Curr Protein Pept Sci. 2013;14(8):641-9. doi: 10.2174/138920371408131227155308