Número: 5.5 - 4 Artigo(s)
- Imprimir
- Indicar
- Estatísticas
- (0) Comentários
- Como Citar
- Download Citação
- Artigos Relacionados
- Outros dos Autores
Relato de Caso
Enxerto ósseo homólogo na reconstrução maxilar para reabilitação de paciente fissurado com implante dentário
Bone Allografts on Maxillary Reconstruction for Oral Rehabilitation with Dental Implants in Cleft Lip and Palate Patients
Plínio Campana e Souza, Mayra Mattos Gomes, Hugo Chaves de Oliveira, Mateus Antunes Ribeiro, Hugo Leite Rodrigues Neto, Rodrigo Guerra de Oliveira
Resumo
FUNDAMENTAÇÃO. A reabilitação oral de pacientes fissurados é um grande desafio a Odontologia devido às opções de reabilitação convencionais (próteses parciais fixas ou removíveis).
OBJETIVO. Relatar um caso de um paciente fissurado submetido a procedimento de enxertia com osso homólogo para posterior reabilitação com implantes dentários.
RELATO DE CASO. Homem, 24 anos, fissurado apresentou-se para reabilitação com implante osseointegrável. O paciente apresentava elementos decíduos 52 e 53 e agenesia do 12°, além de grave defeito ósseo maxilar na região da agenesia, contudo sem apresentar fístula oronasal (fenda pré-forame unilateral). Realizou-se esvaziamento do canal incisivo e preenchimento com osso liofilizado inorgânico GEN-OX® (BAUMER).
RESULTADOS. O defeito maxilar foi preenchido com osso homólogo. O complexo enxertivo foi coberto por membrana de colágeno GEN-DERM® (BAUMER).
CONCLUSÃO. Dentro das limitações desse estudo, pode-se concluir que os procedimentos de enxertia em pacientes fissurados apresentam grande taxa de sucesso cirúrgico, fornecendo bases fortes para uma reabilitação oral plena, dos pontos de vista funcional, estético e social, promovendo maior satisfação do paciente.
Palavras-chave: implantes dentários, cavidade oral, enxerto ósseo.
FUNDAMENTAÇÃO
A reabilitação de pacientes fissurados é um grande desafio para a Implantodontia, uma vez que esses pacientes requerem procedimentos de enxertia óssea não só para alcançar suporte ósseo suficiente para instalação de implantes osseointegráveis, mas também para a obtenção de uma altura óssea apropriada para a estética da prótese6,10,15,18,19,23,24.
A enxertia óssea é o procedimento de eleição para fechamento de fístula oronasal3,4,6,8,12,14,18,19,25 e, com isso, permitir a erupção dentária no local, prover suporte ósseo para os elementos dentários adjacentes, estabilizar a pré-maxila e criar suporte para a base alar6,18,19.
A reabilitação desses pacientes através de próteses convencionais apresenta problemas funcionais, estéticos e sociais2,6,10,19,23. Além de contornar esses fatores, a reabilitação com implantes dentários nessas áreas promove estimulação óssea, prevenindo a reabsorção do enxerto e garantindo a longevidade dos benefícios2,6,18,23.
Com a introdução dos implantes dentários, a qualificação dos profissionais e das biotecnologias envolvidas, ampliou-se as indicações das reabilitações orais, modificando o tratamento em diversos quadros de edentulismo parcial ou total2,6,18,19. Dessa forma, os problemas odontológicos que, historicamente, eram os mais difíceis de serem solucionados, podem hoje ser resolvidos com maior eficiência2,6.
Fenda palatina e lábio leporino estão entre as mais frequentes malformações congênitas, com incidência de 1/10003,4,6,8,11,12,14,25. Aproximadamente 75% dos casos incluem defeito no osso alveolar maxilar, sendo que a enxertia óssea, que é a terapia de eleição, faz-se necessária em 30% a 40% dos pacientes3,4,6,11.
Relativamente à classificação dos vários tipos de fendas, Kernahan et al. (1958) identificaram três grupos principais: I) Fendas do palato primário – lábio e rebordo alveolar; II) Fendas do palato secundário – palato duro e palato mole; III) Fendas do palato primário e secundário - lábio, alvéolo dentário e palato duro e mole.
Outra classificação, uma das mais utilizadas atualmente, é a de Spina et al. (1972) modificada, por ser simples, objetiva e prática o suficiente para facilitar a comunicação entre profissionais de uma equipa multidisciplinar. Esta classificação compreende quatro diferentes grupos e tem como ponto de referência anatômico o forame incisivo que separa o palato primário do palato secundário. I) Fendas pré-forame incisivo: Unilateral (incompleta ou completa); Bilateral (incompleta ou completa); Mediana (incompleta ou completa). II) Fendas transforame incisivo: Unilateral; Bilateral; Mediana. III) Fendas pós-forame incisivo: Incompleta; ou Completa. IV) Fendas raras da face. É necessário ter em conta que as pré-forame estão relacionados com a estrutura lábios e alvéolos e, que, as transforame e as pós-forame se relacionam com o palato duro e o mole.
Se o procedimento de enxertia for realizado antes da erupção do canino, a movimentação ortodôntica permite o fechamento completo em 90% dos casos, sendo somente em 10% necessária reconstrução protética. Se a enxertia se dá após a erupção do canino, a possibilidade de fechamento pela mecânica ortodôntica é reduzida a 72%, aumentando a demanda protética4,6,20.
Devido a essa indicação de terapia ortodôntica, quanto à escolha dos materiais para enxertia, substitutos ósseos como hidroxiapatita e osso liofilizado não são considerados adequados, uma vez que não permitem a movimentação dentária, seja natural (erupção) ou ortodôntica1,6,7,10,20,22.
Os pacientes fissurados frequentemente apresentam agenesias, principalmente de incisivos laterais10,17. Por isso, destaca-se a importância da intervenção ortodôntica, promovendo o fechamento do diastema pela mesialização do dente posterior a falha. Já em pacientes com agenesia de mais de um dente, esse fechamento exclusivamente ortodôntico é praticamente impossível, levando a necessidade de reabilitação protética10,20.
O método mais frequente de reabilitação são as próteses parciais fixas e removíveis6,18,19,23. Contudo, por requererem desgaste de elementos dentários sadios e apresentar dificuldades funcionais, estéticas e/ou sociais, necessitou-se de uma outra opção terapêutica para a efetiva resolução desses casos. A grande taxa de sucesso dos implantes osseointegráveis propiciou essa nova possibilidade reabilitadora, desde que realizado um correto preparo do sítio receptor, através de técnicas corretas de enxertia óssea, e após o término de crescimento da região orofacial2,6,18,23.
Três fatores devem ser analisados quando da realização de enxertia óssea como preparo do sítio receptor para implantes4,6: 1) Extensão do defeito ósseo – o defeito ósseo pode ser incompleto ou completo (se apresentar fístula oronasal); 2) Tecidos moles adjacentes – apresentam sempre baixa qualidade, resultado do defeito congênito, hipoplasia e fibrose por cicatrizes; 3) Material de preenchimento – deve-se considerar que dois materiais devem ser combinados: um que preencha o defeito ósseo e outro que sirva de arcabouço para o primeiro.
Apesar de existirem vários tipos de materiais para enxertia, o de eleição é o osso autógeno, por prover células osteogênicas (importantes no primeiro estágio da formação óssea) e não ativar a resposta imunológica1,5,7,15,16,22,23,24. As principais desvantagens do osso autógeno são a necessidade de outro sítio cirúrgico, elevando a morbidade do procedimento como um todo, e a disponibilidade de quantidade de material dos sítios doadores1,5,7,15,23.
Com isso, a procura por uma alternativa viável ao osso autógeno levou ao osso homólogo (alógeno). Apesar de diminuir a morbidade cirúrgica, o osso homólogo possui como principal desvantagem não possuir células osteogênicas (perdidas durante o processo de preparação, para não ativar resposta imunológica), não participando da primeiro estágio de osteoformação. Sua contribuição ocorre somente na segunda fase da osteogênese (osteoindução) sendo puramente passiva, servindo somente como arcabouço1,5,7,10,15,16,23,24
Mediante o exposto, o presente artigo, procurou relatar o procedimento de enxertia óssea em um paciente fissurado, visando à correção do leito receptor para posterior reabilitação com implante dentário.
MÉTODOS
Paciente do sexo masculino, 24 anos, fissurado (Fig. 1A, 1B) apresentou-se a clínica de um curso de pós-graduação em Implantodontia para reabilitação com implante osseointegrável. Ele havia sido submetido a um tratamento ortodôntico prévio durante 26 meses. O paciente apresentava elementos decíduos 52 e 53 e agenesia do 12. Mediante tomografia computadorizada (TC) da região, foi detectado grave defeito ósseo maxilar na região da agenesia (Fig. 1C), com comunicação do defeito ósseo com o canal incisivo (Fig. 1D, 1E), contudo, sem apresentar fístula oronasal (fenda pré-forame unilateral).
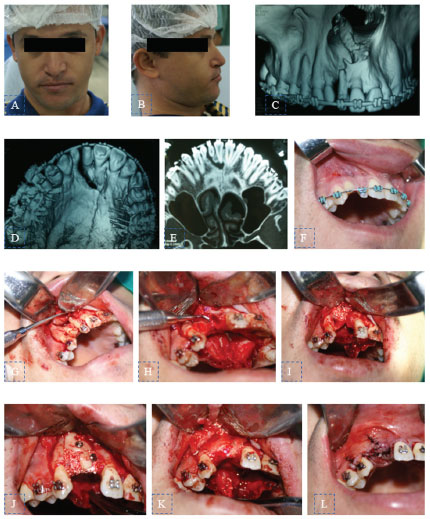
Figure 1. Procedimento de enxertia homóloga em paciente fissurado. A, Vista frontal; B, Vista lateral; C, TC – vista frontal; D, TC – vista oclusal; E, TC – corte demonstrando comunicação do defeito ósseo com o canal incisivo; F, vista intra-oral; G, Descolamento e exposição do sítio receptor. Presença dos elementos decíduos 52 2 53 e agenesia do elemento 22; H, Sonda demonstrando a comunicação do defeito ósseo com o canal incisivo; I, Preenchimento do defeito com osso liofilizado bovino inorgânico; J, Fixação dos dois blocos de osso homólogo; K, Adaptação da membrana de colágeno; L, Fechamento pós-sutura.
Com base nos dados dos exames complementares, foi realizado o planejamento cirúrgico para correção do sítio implantar. A proposta apresentada ao paciente incluía o uso de enxerto de osso autógeno (obtido da região de ângulo mandibular) e osso liofilizado inorgânico. Contudo, conforme objeção do paciente, optou-se pelo uso de osso homólogo e liofilizado inorgânico. Apesar das diferenças entre as propriedades dessas opções de enxertia, não haveria comprometimento do resultado final, uma vez que não seria mais realizada movimentação ortodôntica no local.
RESULTADOS
Após incisão intrasulcular com retalho mucoperiosteal total (Fig. 1G), procedeu-se a exodontia dos elementos decíduos e curetagem do defeito ósseo, para remoção de quaisquer remanescentes teciduais aderidos internamente a falha. Secundariamente realizou-se esvaziamento do canal incisivo e preenchimento com osso liofilizado bovino inorgânico (Fig. 1H, 1I) GEN-OX® (BAUMER). O defeito maxilar foi preenchido com osso homólogo de cortical de patela (proveniente de Banco de Ossos de Marília) e osso liofilizado inorgânico GEN-OX® (BAUMER), sendo os blocos fixados por parafusos de fixação de enxerto (Fig. 1J) de 12 mm e 10 mm (SIN). O complexo enxertivo foi coberto por membrana de colágeno GEN-DERM® (BAUMER) para proteção da área (Fig. 1K). Procedeu-se então ao fechamento do sítio cirúrgico sem tensão, para evitar exposição durante a cicatrização, com suturas simples e mesodermais horizontais e verticais (Fig. 1L).
DISCUSSÃO
Apesar de vários estudos sobre enxertia óssea demonstrarem excelentes resultados histológicos, radiográficos e clínicos1,6,15,18 poucos trabalhos examinaram esses resultados em enxertos realizados em pacientes fissurados10,13. Uma importante dificuldade nesses pacientes é a fixação do enxerto ósseo, já que a instabilidade pode promover sua reabsorção5,6,7,15. Isso leva a uma altura óssea alveolar insuficiente e um grande volume de enxerto torna-se necessário1,10,15,18. Além disso, frequentemente, a altura óssea adquirida é insuficiente, requirindo nova enxertia10,15.
Outra dificuldade é a perda de elasticidade do tecido mole adjacente, devido ao fibrosamento cicatricial de outras cirurgias no local4,6,18 o que leva a uma grande dificuldade de fechamento por primeira intenção. Devido as suas propriedades biológicas, o material de enxertia padrão ouro é o osso autólogo, permitindo a continuidade de todos os processos fisiológicos locais4,5,6,7,15,22,23,24. Contudo, estudos demonstraram grande índice de reabsorção nessa região de fendas ósseas. A razão para isso é atribuída a provável compressão resultante do lábio superior e movimentação durante a fonação4.
Apesar de suas limitações fisiológicas1,5,7,15,16,23,24 o osso homólogo apresentou grande taxa de sucesso nesses pacientes, inclusive apresentando menor nível de reabsorção quando comparados aos autólogos1,5,7,15,24, mas os mecanismos responsáveis por tais diferenças ainda são desconhecidos.
Existem vários produtos no mercado designados a substituir o osso humano (autólogo ou homólogo). Cada profissional deve selecionar o melhor produto, segundo suas características e estudos realizados sobre ele, para cada caso clínico1,7,10,15,20,22.
Após anos de pesquisa, como nenhuma substância com propriedades equivalentes ao osso autógeno foi encontrada, seguem-se estudos para maior compreensão do processo de incorporação dos enxertos, com finalidade de desenvolver um substituto ideal, diminuindo, dessa forma, a morbidade cirúrgica para o paciente1,5,7,15,16,22,24.
Muitos estudos relatam as experiências com implantes osseointegráveis em pacientes fissurados6,10,18,19,24. Contudo, na maioria dos estudos a amostra era pequena e o período de acompanhamento era relativamente curto10,18. Devido a essas limitações, fatores de risco potenciais a perda de implantes nesses pacientes são difíceis de serem determinados. Além disso, há carência de estudos comparando o índice de sucesso de implantes em pacientes fissurados e não-fissurados10.
CONCLUSÃO
Os procedimentos de enxertia em pacientes fissurados, com finalidade de preparo do sítio receptor para posterior instalação de implantes osseointegráveis, apresentam grande taxa de sucesso cirúrgico, fornecendo bases fortes para uma reabilitação oral plena, dos pontos de vista funcional, estético e social, promovendo maior satisfação do paciente.
Os enxertos com osso homólogo para essas situações podem ser realizados com segurança e significativa taxa de sucesso, desde que corretamente empregados conforme o tipo de plano de tratamento reabilitador proposto pelo profissional.
REFERÊNCIAS
1. Baptista DA, Sorrilha A, Tormes TAM, Abdcune YA, Croci AT, Camargo OP et al. Estudo histológico dos enxertos ósseos homólogos humanos. Acta Ortop Bras 2003; 11: 220-4.
2. Block MS, Baughman DG. Reconstruction of severe anterior maxillary defects using distraction osteogenesis, bone grafts, and implants. J Oral Maxillofac Surg 2005; 63:291-7.
3. Corbo M, Dujardin T, de Maertelaer V, Malevez C, Glineur R. Dentocraniofacial morphology of 21 patients with unilateral cleft lip and palate: a cephalometric study. Cleft Palate Craniofac J. 2005; 42: 618-24.
4. Duskova M, Kotova M, Sedlackova K, Leamerova E, Horak J. Bone reconstruction of the maxillary alveolus for subsequent insertion of a dental implant in patients with cleft lip and palate. J Craniofac Surg. 2007; 18: 630-8.
5. Ellis III E, Sinn DP. Use of homologous bone in maxillofacial surgery. J Oral Maxillolac Surg 1993; 51: 1181-93.
6. Genden EM. Reconstruction of the mandible and the maxilla: the evolution of surgical technique. Arch Facial Plast Surg 2010; 12: 87-90.
7. Goiato MC, Anchieta RB, Pita MS, Santos DM. Reconstruction of skull defects: currently available materials. J Craniofac Surg 2009; 20: 1512-1518.
8. Honda Y, Suzuki A, Nakamura N, Ohishi M. Relationship between primary palatal form and maxillofacial growth in Japanese children with unilateral cleft lip and palate: infancy to adolescence. Cleft Palate Craniofac J 2002; 39:527-34.
9. Kernahan DA, Stark RB. A new classification for cleft lip and palate. Plast Reconstr Surg Transplant Bull 1958; 22: 435-41.
10. Kramer FJ, Baethqe C, Swennen G, Bremer B, Schwestka-Polly R, Dempf R. Dental implants in patients with orofacial clefts: a long-term follow-up study. Int J Oral Maxillofac. Surg 2005; 34: 715–21.
11. Liao YF, Mars M. Long-term effects of clefts on craniofacial morphology in patients with unilateral cleft lip and palate. Cleft Palate Craniofac J 2005; 42: 601-9.
12. Liao YF, Mars M. Long-term effects of palate repair on craniofacial morphology in patients with unilateral cleft lip and palate. Cleft Palate Craniofac J 2005; 42: 594-600.
13. Mulliken JB, Wu JK, Padwa BL. Repair of bilateral cleft lip: review, revisions, and reflections. J Craniofac Surg 2003; 14:609-20.
14. Nakamura N, Suzuki A, Takahashi H, Honda Y, Sasaquri M, Ohishi M. A longitudinal study on influence of primary facial deformities on maxillofacial growth in patients with cleft lip and palate. Cleft Palate Craniofac J 2005; 42:633-40.
15. Peleg M, Sawatari Y, Marx RN, Santoro J, Cohen J, Bejarano P, Malinin T. Use of corticocancellous allogeneic bone blocks for augmentation of alveolar bone defects. Int J Oral Maxillofac Implants 2010; 25: 153-63.
16. Precheur HV. Bone graft materials. Dent Clin N Am 2007; 3:729–746
17. Rosenstein SW, Grasseschi M, Dado DV. A long-term retrospective outcome assessment of facial growth, secondary surgical need, and maxillary lateral incisor status in a surgical-orthodontic protocol for complete clefts. Plast Reconstr Surg 2003; 111-1-13.
18. Sawaki M, Ueno T, Kagawa M, Kanou M, Honda K, Shirasu N et al. Dental implant treatment for a patient with bilateral cleft lip and palate. Acta Med Okayama 2008; 62: 59-62.
19. Sawaki M, Ueno T, Kagawa T, Mizukawa N, Kanou M, Sakata Y. Clinical investigation of dental implant reconstruction for grafted alveolar cleft patients. Journal of Hard Tissue Biology 2007; 16:87-90.
20. Schultes G, Gaggl A, Kärcher H. A comparison of growth impairment and orthodontic results in adult patients with clefts of palate and unilateral clefts of lip, palate and alveolus. Br J Oral Maxillofac Surg 2000; 38: 26-32.
21. Spina V. Classificação das fissuras lábio-palatinas: sugestão de modificação. Rev Hosp Fac Med S Paulo 1972; 27: 5-6.
22. Tatum SA, Losquadro WD. Advances in craniofacial surgery. Arch Facial Plast Surg 2008; 10:376-380.
23. Viscioni A, Rigo L, Franco M, Brunelli G, Avantaqqiato A, Sollazzo V et al . Reconstruction of severely atrophic jaws using homografts and simultaneous implant placement: a retrospective study. Journal of Oral Implantol 2010; 36: 131-9.
24. Waasdorp J, Reynolds MA. Allogeneic bone onlay grafts for alveolar ridge augmentation: a systematic seview. Int J Oral Maxillofac Implants 2010; 25: 525-31.
25. Yamada T, Mori Y, Mishima K, Sugahara T. Nasolabial and alveolar morphology following presurgical orthopaedic treatment in complete unilateral clefts of lip, alveolus and palate. J Craniomaxillofac Surg 2003; 31: 343-7.



