Número: 7.7 - 6 Artigo(s)
- Imprimir
- Indicar
- Estatísticas
- (0) Comentários
- Como Citar
- Download Citação
- Artigos Relacionados
- Outros dos Autores
Artigos de Revisão
Trombocitopenia Aloimune Fetal/Neonatal: Uma Revisão Sistemática
Fetal/Neonatal Alloimmune Thrombocytopenia: A Systematic Review
Julianna Oliveira de Lucas Xavier1; Letticya Ribeiro de Almeida Batista1; Patricia Guedes Garcia2; Ana Paula Ferreira2
1. Estudante do Programa de Pós – Graduação em Análises Clínicas da Faculdade de Ciências Médicas e da Saúde de Juiz de Fora – SUPREMA
2. Doutora, Professora da Faculdade de Ciências Médicas e da Saúde de Juiz de Fora – SUPREMA
E-mail: xavierjulianna@gmail.com
Resumo
INTRODUÇÃO: A trombocitopenia aloimune fetal e neonatal (FNAIT) é causada por incompatibilidade de antígenos plaquetários entre mãe e feto, que resulta em respostas imunológicas mediadas por anticorpos. O organismo da mãe produz anticorpos contra antígenos plaquetários fetais específicos. Esses anticorpos atravessam a placenta e ligam-se às plaquetas fetais, removendo-as da circulação através do sistema reticuloendotelial.
OBJETIVO: Analisar, por meio de revisão sistemática, os casos de FNAIT para verificar a classe de antígenos plaquetários mais envolvida com a patologia e compreender as medidas preventivas adotadas durante a gestação.
MÉTODO: Foi realizada uma busca de artigos científicos dos últimos 10 anos. A base de dados utilizada foi o PubMed, sendo os descritores “Thrombocytopenia, Neonatal Alloimmune” e “Clinical Laboratory Techniques” determinados pelo MesH (Medical Subject Headings). Foram aplicados critérios de inclusão com base na data de publicação, espécie e idioma. Os artigos considerados não relevantes e estudos do tipo “Relatos de Caso” foram excluídos.
RESULTADOS: Foram selecionados para fazer parte do escopo desta revisão 7 artigos, que apontaram as incompatibilidades envolvendo o HPA-1a como as principais responsáveis pelos quadros de FNAIT. Com relação aos tratamentos pré-natais oferecidos às gestantes, observou-se uma variabilidade nas estratégias terapêuticas, mas o emprego da imunoglobulina intravenosa associada ou não à corticosteróides têm se mostrado eficaz para a prevenção de hemorragia intracraniana e óbitos de fetos/neonatos.
CONCLUSÃO: Os casos de FNAIT, apesar de raros, são graves e mostraram-se de difícil diagnóstico e manejo clínico. Portanto, há necessidade de desenvolvimento contínuo de novos estudos que auxiliem no diagnóstico e na padronização de métodos preventivos.
Palavras-chave: Trombocitopenia Neonatal Aloimune, Imunização, Hemorragias Intracranianas, Morte Fetal.
INTRODUÇÃO
A trombocitopenia aloimune fetal e neonatal (do inglês, fetal and neonatal alloimmune thrombocytopenia [FNAIT]) é a causa mais comum de trombocitopenia em neonatos e afeta entre 1/800 e 1/1000 nascidos vivos, sendo que a ocorrência de casos graves (contagem de plaquetas <50.000/mm³) causados por anticorpos anti-HPA-1a é de aproximadamente 1/2500 gestações1-3.
A FNAIT é causada por uma incompatibilidade de antígenos plaquetários entre a mãe e o feto, que resulta em respostas imunológicas mediadas por anticorpos. O organismo da mãe produz anticorpos do tipo imunoglobulina G (IgG) contra antígenos plaquetários fetais específicos que são de origem paterna. Esses anticorpos produzidos atravessam a barreira placentária e ligam-se às plaquetas fetais que, posteriormente, serão removidas da circulação pelo sistema reticuloendotelial resultando em trombocitopenia fetal1,4.
A aloimunização ocorre para um ou mais antígenos plaquetários humanos (do inglês, human platelet antigens [HPA]). Esses antígenos estão situados nas glicoproteínas plaquetárias, sendo a maioria localizada na glicoproteína transmembrana GPIIb/IIIa. Foi constatado que os anticorpos envolvidos com FNAIT estão relacionados com seis tipos de antígenos bialélicos (HPA-1, HPA-2, HPA-3, HPA-4, HPA-5 e HPA-15). Os diferentes alelos de HPA variam de acordo com os grupos étnicos, sendo o anticorpo contra HPA-1a o mais prevalente em caucasianos, responsável por 70 a 85% dos casos de FNAIT nessa população5.
Os bebês que desenvolvem FNAIT apresentam trombocitopenia, petéquias e hematomas. Além disso, cerca de 10% dos casos podem evoluir para hemorragia intracraniana (do inglês, intracranial hemorrhage [ICH]), a complicação mais grave e que pode levar a óbito ou incapacidade neurológica em aproximadamente 90% dos casos6,7.
Como não há triagem de rotina para todas as gestantes, não há como prever a ocorrência de FNAIT atualmente. Portanto, para reduzir os casos de complicações para ICH, o método de intervenção é o tratamento de gestações subsequentes a uma gestação anterior identificada com FNAIT. Contudo, apenas 13% dos casos são diagnosticados utilizando-se esse histórico obstétrico como um preditor. Nos exames pré-natais são adotadas medidas preventivas para gestações de risco, como a infusão semanal de imunoglobulina intravenosa (IVIG) para a mãe, associada ou não a corticosteróides, e transfusão intrauterina de plaquetas. Inicialmente, é colhida uma amostra de sangue fetal para contagem de plaquetas e, depois, caso necessário, é realizada a transfusão intrauterina de plaquetas compatíveis. Entretanto, essas medidas estão associadas a partos prematuros e abortos em 1 a 2% dos procedimentos2,7.
Dada a gravidade de FNAIT e o desafio para o seu diagnóstico ainda no período pré-natal, o objetivo desta revisão sistemática foi analisar, sob uma perspectiva laboratorial e terapêutica, os casos de trombocitopenia aloimune fetal e neonatal para verificar a classe de antígenos plaquetários mais envolvida nos casos e compreender as medidas preventivas adotadas durante o período gestacional.
MÉTODOS
Estratégias de pesquisa
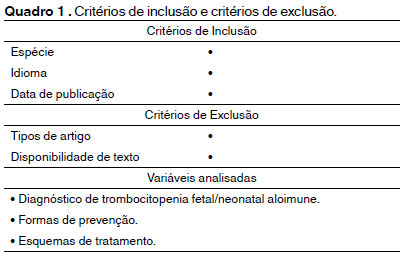
Foi realizada uma busca de artigos científicos dos últimos 10 anos, até 31 de agosto de 2019. A base de dados utilizada foi o PubMed, sendo os descritores “Thrombocytopenia, Neonatal Alloimmune” e “Clinical Laboratory Techniques” determinados pelo MesH (Medical Subject Headings). Utilizando-se a ferramenta de busca avançada através dos operadores booleanos “OR” e “AND” foram encontrados 763 artigos. Em seguida, foram aplicados alguns critérios de inclusão com base na data de publicação, espécie e idioma. Os artigos considerados não relevantes e estudos do tipo “Relatos de Caso” foram excluídos (Quadro 1).
RESULTADOS
Foram identificados 763 artigos científicos envolvendo a trombocitopenia neonatal/fetal aloimune e técnicas laboratoriais clínicas. Porém, após a aplicação dos critérios de inclusão previamente estabelecidos, restaram 227 estudos para leitura dos títulos. Excluindo-se aqueles considerados não relevantes, foram eleitos 79 artigos para leitura dos resumos e foram excluídos estudos do tipo “Relato de Caso”. Por fim, foram selecionados para fazer parte do escopo desta revisão sistemática 7 artigos. A Figura 1 apresenta o fluxograma de processo de seleção de artigos.
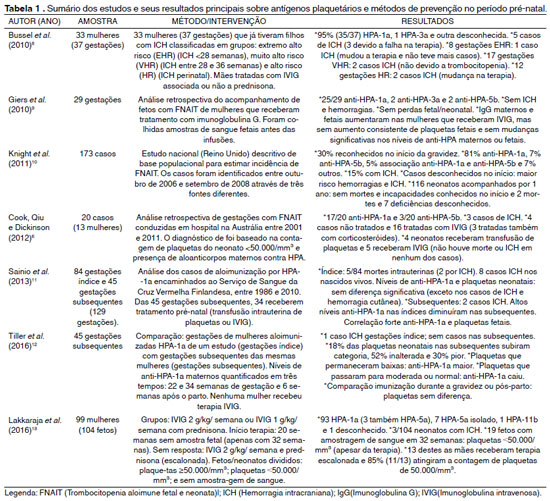
Em geral, os estudos analisados envolveram diferentes abordagens, como: I) análises retrospectivas de casos de FNAIT ou aloimunização por HPA-1a; II) estudos de acompanhamento de mulheres que receberam tratamentos pré-natais em suas gestações, pois já tiveram filhos com ICH; e III) comparações entre gestações anteriores e gestações subsequentes das mesmas mulheres que apresentaram filhos com FNAIT (Tabela 1).
Conforme já vêm sido descrito na literatura, todos os estudos do escopo desta revisão sistemática apontaram as incompatibilidades envolvendo o antígeno HPA-1a como as principais responsáveis pelos quadros de FNAIT, com prevalências variando de 85 a 95% dos casos. Os autores demonstraram a importância de uma avaliação mais aprofundada dos históricos de FNAIT ou ICH em gestações anteriores para serem adotadas medidas preventivas para gestações subsequentes. Com relação aos tratamentos pré-natais oferecidos às gestantes, pôde-se observar uma variabilidade nas estratégias terapêuticas adotadas pelos hospitais ou centros de terapias, mas, apesar dessa heterogeneidade, o emprego da IVIG associada ou não à corticosteróides têm se mostrado eficaz para a prevenção de ICH e óbitos de fetos ou neonatos.
DISCUSSÃO
Os resultados mostraram a importância de métodos preventivos no período pré-natal para gestantes que apresentaram histórico de ICH ou FNAIT em gestações anteriores, apesar dos esquemas terapêuticos envolvendo IVIG e corticosteróides variarem entre os estudos.
Eficácia das terapias no período pré-natal para prevenção de ICH ou óbitos em fetos/neonatos
Os estudos demonstraram a importância das terapias com imunoglobulina intravenosa, associadas ou não a corticosteróides e transfusões intrauterinas de plaquetas, para minimizar ocorrências de complicações hemorrágicas, como a ICH, que podem resultar em óbitos de fetos/neonatos.
Isso pode ser demonstrado no estudo de Cook et al. (2012)6, no qual 16 mulheres foram tratadas com IVIG 1 g/kg/semana, sendo que três delas receberam associação com corticosteróide (prednisolona), quatro neonatos receberam transfusão de plaquetas e cinco receberam IVIG após o nascimento e não houve ICH ou morte nesses casos. Uma abordagem parecida foi realizada no estudo de Giers et al. (2010)9 onde as gestantes também foram tratadas com IVIG 1 g/kg/semana, mas, antes do parto, os fetos receberam transfusão intrauterina de plaquetas: não houve complicações hemorrágicas e nem óbitos, apesar de não apresentar aumento consistente da contagem de plaquetas fetais.
Já no trabalho de Lakkaraja et al. (2016)13, cujo objetivo fora avaliar se a terapia empírica seguida por escalonamento seria eficaz e permitiria omissão de coleta de sangue fetal, foram criados dois grupos de tratamento: I) IVIG 2 g/kg/semana dividia em duas infusões na semana e II) IVIG 1 g/kg/semana com prednisona 0,5 mg/kg/dia, como terapias empíricas iniciadas sem amostragem fetal, sendo esta realizada somente na 32ª semana de gestação. Neste protocolo, os que não respondessem à terapia na amostragem fetal, tiveram um aumento para IVIG 2 g/kg/semana e prednisona 0,5 mg/kg/dia (terapia escalonada). Portanto, após a coleta de sangue fetal, 19/104 fetos apresentaram plaquetas <50.000/mm³ e 13 receberam a terapia escalonada: 11 destes nasceram com plaquetas >50.000/mm³ e 3/104 neonatos sofreram ICH pós-natal. Então, estes autores concluíram que o aumento na contagem de plaquetas fetais ocorreu em quase todos os casos e que essas duas formas de tratamento inicial seguida por escalonamento são razoavelmente seguras e eficazes.
Bussel et al. (2010)8, que estudaram a prevenção de ICH através de terapia pré-natal com gestantes de dois estudos consecutivos, classificaram as mulheres em grupos de risco e formas diferentes da terapia foram adotadas, sendo realizados ajustes nas dosagens: por exemplo, uma gestante do grupo de extremo alto risco foi tratada com IVIG 1 g/kg/semana e prednisona 1 mg/kg/dia mas, após perder o bebê, as próximas gestantes deste grupo foram tratadas com IVIG 2 g/kg/semana dividias em duas doses. As gestações do primeiro estudo do grupo muito alto risco receberam IVIG 1 g/kg/semana e no segundo estudo IVIG 1 g/kg/semana ou 2 g/kg/semana. E, por fim, as gestações do grupo alto risco no primeiro estudo receberam IVIG 1 g/kg /semana e prednisona 1 mg/kg/dia ou IVIG 1 g/kg/semana apenas e, no segundo estudo, IVIG 1 g/kg/semana ou IVIG 2 g/kg/semana.
Através da análise desses estudos tomados como exemplo, percebe-se que são adotados diferentes métodos de prevenção de complicações hemorrágicas que podem evoluir para perdas dos fetos/neonatos, com variações nas dosagens de imunoglobulina intravenosa assim como o corticosteróide utilizado (prednisona ou prednisolona) e suas dosagens.
Técnicas laboratoriais para diagnóstico de FNAIT
Com relação às técnicas empregadas pelos autores para identificação e quantificação dos anticorpos contra HPA, Giers et al. (2010)9, Sainio et al. (2013)11 e Tiller et al. (2016)12 utilizaram o teste de imobilização de antígenos plaquetários por anticorpos monoclonais (MAIPA).
O MAIPA é um ensaio que utiliza um painel de plaquetas de doadores com genotipagem conhecida e anticorpos monoclonais específicos contra as glicoproteínas que contêm os antígenos alvo, ou seja, ao se utilizar anticorpo monoclonal contra a glicoproteína IIbIIIa, avalia-se a presença de anticorpos contra antígenos específicos deste complexo, como o HPA-1 e HPA-3. Como se trata de uma técnica totalmente “in-house”, requer uma boa padronização através da utilização de controles internos e externos. Além disso, é um ensaio tecnicamente exigente, podendo necessitar de até 8 horas para sua realização e requer alto nível de conhecimento técnico para a interpretação de seus resultados. Por este motivo, outros métodos para detecção desses anticorpos vêm sido desenvolvidos14,15.
Além desta, outras técnicas também são empregadas, como testes de imunofluorescência plaquetária (do inglês, platelet imunofluorescence test [PIFT]) e ELISA (do inglês, enzyme-linked immunosorbent assay) baseada no uso de glicoproteínas de membrana de plaquetas purificadas. Porém, como o MAIPA é a técnica mais sensível e específica para detecção de aloanticorpos contra HPA, vem sendo considerada o método padrão ouro para o diagnóstico de FNAIT16,17.
Amostragem fetal e suas complicações
Autores de dois estudos apontaram complicações associadas ao procedimento de coleta de amostras de sangue fetal. Por exemplo, Bussel et al. (2010)8 relataram que esta pode ter sido a causa de um parto prematuro com 24 semanas de gestação. Além disso, após a coleta de sangue fetal, houve uma ocorrência de taquicardia fetal e oito ocorrências de bradicardia, sendo que em três destes casos foi necessária cesariana de emergência, no qual um deles foi devido à hemorragia no local de perfuração da agulha. Já no estudo de Lakkaraja et al. (2016)13, que inclusive teve como objetivo avaliar se a coleta de sangue fetal pode ser omitida através de terapia empírica, de oitenta mulheres que foram submetidas ao procedimento, 12,5% (10) sofreram complicações, como parto prematuro ou ruptura de membranas em seis casos e, nos restantes quatro casos, realizada cesariana por bradicardia fetal. Por fim, estes autores concluíram que os protocolos de tratamentos iniciais seguidos por escalonamento empírico da terapia é razoavelmente seguro, eficaz no aumento de plaquetas fetais e permite a omissão da coleta de sangue fetal.
CONCLUSÃO
A presente revisão mostra que a maioria dos casos de incompatibilidade mãe/feto de antígenos plaquetários envolveu a classe anti-HPA-1a, conforme já vem sido descrito na literatura. Além disso, o estudo demonstra uma variabilidade nas estratégias terapêuticas adotadas para prevenção em gestações de risco, mas, apesar disso, o emprego da IVIG associada ou não à corticosteróides mostrou-se eficaz para a prevenção de ICH e óbitos de fetos ou neonatos.
Os casos de FNAIT, apesar de raros, são graves e mostraram-se de difícil diagnóstico e manejo clínico. Portanto, há a necessidade de desenvolvimento contínuo de novos estudos que auxiliem no diagnóstico da doença e na padronização de métodos preventivos eficazes durante o período pré-natal.
REFERÊNCIAS
1. Kamphuis MM, Oepkes D. Fetal and neonatal alloimmune thrombocytopenia: prenatal Interventions. Prenat Diagn 2011; 31:712-719.
2. Kjær M, Bertrand G, Bakchoul T, Massey E, Baker JM, Lieberman L, et al. Maternal HPA-1a antibody level and its role in predicting the severity of fetal/neonatal alloimmune thrombocytopenia: a systematic review. Vox Sanguinis 2019; 114:79-94.
3. Poles A, Lucas G, Green F, Walser P, Davey S, Ridgwell K, et al. Neonatal alloimmune thrombocytopenia due to a new alloantigen Bl(a) defined by an Asp458Gly substitution in GPIIIa. Transfusion 2019; 59:396-404.
4. Refsum E, Meinke S, Gryfelt G, Wikman A, Höglund P. Adding to the complexity of fetal and neonatal alloimmune thrombocytopenia: reduced fibrinogen binding in the presence of anti-HPA-1a antibody and hypo-responsive neonatal platelets. Thrombosis Research 2018; 162:69-76.
5. Bonstein L, Haddad N. Taking a wider view on fetal/neonatal alloimmune thrombocytopenia. Thrombosis Research 2017; S100-S102.
6. Cook TJ, Qiu CC, Dickinson JE. A review of the contemporary management of fetal and neonatal alloimmune thrombocytopenia in an australian tertiary obstetric hospital. Australian and New Zealand Journal of Obstetrics and Gynaecology 2012; 52:321-326.
7. Wienzek-Lischka S, Krautwurst A, Fröhner V, Hackstein H, Gattenlöhner S, Bräuninger A, et al. Noninvasive fetal genotyping of human platelet antigen-1a using targeted massively parallel sequencing. Transfusion 2015; 55;1538-1544.
8. Bussel JB, Berkowitz RL, Hung C, Kolb EA, Wissert M, Primiani A, et al. Intracranial hemorrhage in alloimmune thrombocytopenia: stratified management to prevent recurrence in the subsequent affected fetus. Am J Obstet Gynecol 2010; 203:135.e1-14.
9. Giers G, Wenzel F, Stockschläder M, Riethmacher R, Lorenz H, Tutschek B. Fetal alloimmune thrombocytopenia and maternal intravenous immunoglobulin infusion. Haematologica 2010; 11:1921-1926.
10. Knight M, Pierce M, Allen D, Kurinczuk JJ, Spark P, Roberts DJ, et al. The incidence and outcomes of fetomaternal alloimmune thrombocytopenia: a UK national study using three data sources. British Journal of Haematology 2011; 152:460-468.
11. Sainio S, Javela K, Tuimala J, Koskinen S. Usefulness of maternal anti-HPA-1a antibody quantitation in predicting severity of foetomaternal alloimmune thrombocytopenia. Transfusion Medicine 2013. 23:114-120.
12. Tiller H, Husebekk A, Skogen B, Kjeldsen-Kragh J, Kjær M. True risk of fetal/neonatal alloimmune thrombocytopenia in subsequent pregnancies: a prospective observational follow-up study. BJOG 2016;123:738-744.
13. Lakkaraja M, Berkowitz RL, Vinograd CA, Manotas KC, Jin JC, Ferd P, et al. Omission of fetal sampling in treatment of subsequent pregnancies in fetal-neonatal alloimmune thrombocytopenia. Am J Obstet Gynecol 2016.
14. Wendel RCLF. Avaliação de diferentes metodologias laboratoriais para detecção de aloanticorpos plaquetários. Determinação da prevalência e importância clinica destes aloanticorpos em pacientes transfundidos. 2008. Tese (Doutorado) - Universidade de São Paulo. São Paulo, SP, 2008.
15. Chong W, Turro E, Metcalfe P, Yusuf R, Mérieux Y, Rigal D, et al. A multicenter validation of recombinant b3 integrin-coupled beads to detect human platelet antigen-1 alloantibodies in 498 cases of fetomaternal alloimmune thrombocytopenia. Transfusion 2015; 55:2742-2751.
16. Chong W, Metcalfe P, Mushens R, Lucas G, Ouwehand WH, Navarrete C. Detection of human platelet antigen-1a alloantibodies in cases of fetomaternal alloimmune thrombocytopenia using recombinant b3 integrin fragments coupled to fluorescently labeled beads. Transfusion 2011; 51:1261-1270.
17. Cooper N, Bein G, Heidinger K, Santoso S, Sachs UJ. A bead-based assay in the work-up of suspected platelet alloimmunization. Transfusion 2016;56;115-118.